近日,课题组作为合作单位参与的研究成果“Molecular Identification of Tumor-Derived Extracellular Vesicles Using Thermophoresis-Mediated DNA Computation”于 2021年1月在线发表于《美国化学会志》(J. Am. Chem. Soc. 2020, DOI: 10.1021/jacs.0c12016)。该研究由国家纳米科学中心孙佳姝研究员课题组、上海交通大学韩达课题组、中国人民解放军总医院第五医学中心张少华教授合作,在肿瘤细胞外囊泡DNA分子逻辑运算与乳腺癌分子分型研究方面取得重要进展。
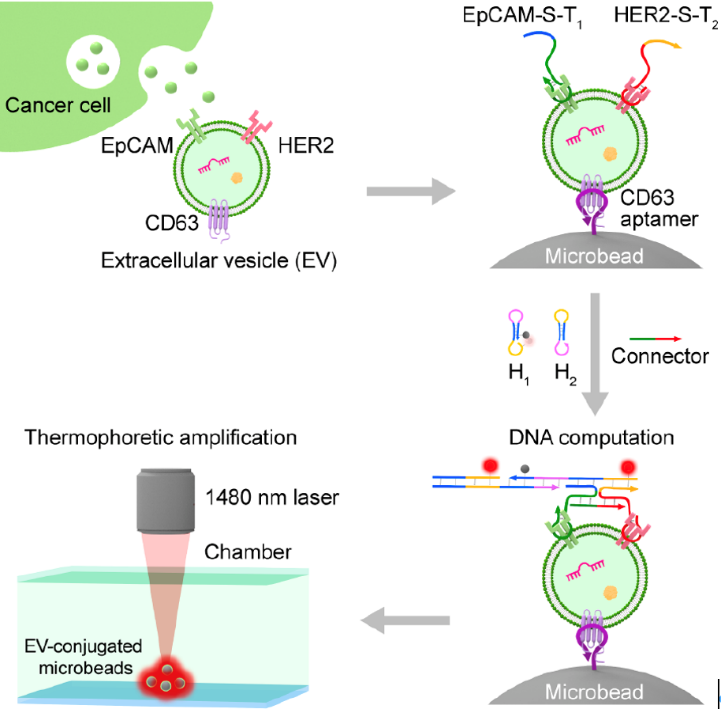
图:基于DNA分子逻辑运算与热泳富集的肿瘤细胞外囊泡精准测量。
细胞外囊泡(Extracellular vesicles,EVs)是肿瘤液体活检的重要靶标之一。前期,孙佳姝课题组致力于高灵敏、高特异的EV分子标志物检测研究,构建了微流控热泳适体监测平台,实现了EV高效富集和蛋白图谱高灵敏检测,并用于癌症早期诊断和分类(Nat. Biomed. Eng. 219, 3, 183-193),并针对EV内miRNA构建了球形核酸分子探针,结合微流控热泳测量平台,实现0.5微升血清样本中EV miRNA高灵敏检测,并用于ER+乳腺癌的早期诊断(JACS 2020, 142, 4996-5001)。韩达课题组在之前的工作中,在细胞膜上构建了多核酸适体的逻辑门装置,实现4种相似肿瘤细胞的精确识别和分离(JACS 2019, 141, 12738-12743),利用滚换扩增技术进行信号放大,进一步提高了细胞识别的特异性和灵敏度,成功应用于临床急性白血病样本中肿瘤细胞亚型的检测(Angew. Chem. 2020, 59, 23564-23568)。
基于前期研究基础,本研究选取泛肿瘤蛋白标志物EpCAM和乳腺癌标志物HER2作为输入信号(Input),构建DNA分子逻辑门(AND),利用杂交链式反应(hybridization chain reaction,HCR)和微流控热泳汇聚放大输出信号(Output),实现了乳腺癌肿瘤EV(HER2+,EpCAM+)的高灵敏精准检测。临床乳腺癌病人血清样本检测结果显示,HER2+,EpCAM+ EV可以提供更丰富准确的肿瘤信息,并用于乳腺癌精准诊断与HER2分子分型。该方法为基于EV的肿瘤液体活检提供了新工具。
论文链接: https://pubs.acs.org/doi/10.1021/jacs.0c12016




